高压均质法制备果胶多柔比星纳米混悬剂
2018-04-21 09:48:16
多柔比星(doxorubicin,DOX)属于蒽环霉素类广谱抗肿瘤药物, 临床上广泛应用于治疗各种恶性肿瘤[1]。与大多数抗肿瘤药物相同,DOX不良反应较多, 较严重的是剂量依赖性心脏毒性,不仅影响了患者的生存质量,而且使DOX的应用受到限制。目前高效低毒的靶向药物研究成为热点。果胶作为天然大分子多聚糖,生物相溶性好,常被用作药物辅料、代血浆和载药载体。所以,选用果胶为载体,将果胶C-6位羧基与DOX C-3'位氨基以酰胺键偶联, 制备果胶多柔比星轭合物(pectin-doxorubicin conjugate,PDC),其重均分子量为6.050×105,数均分子量为2.110×105,见合成路线。PDC在体内通过溶酶体酶作用使共价键断裂, 释放出游离DOX而发挥药效, 达到增效减毒、靶向治疗肿瘤、减少药物毒性的目的。PDC中载体果胶属于天然高分子多聚糖, 结构中含大量的羧基与羟基, 容易产生氢键, 形成刚性结构, 结合小分子DOX后,PDC在水中和有机溶剂中的溶解性差。所以,需要对PDC进行增溶处理。目前常用的共溶剂增溶、环糊精包合、乳剂和微乳等技术存在有机溶剂残留、载药量低、稳定性差及制备工艺复杂等局限性。纳米混悬剂被广泛应用于解决药物因溶解性而限制应用的问题,优点是处方简单,“纯药物”纳米粒增加比表面积, 从而增加药物的溶解度, 提高疗效。所以,本研究拟采用自上而下的高压均质技术将PDC制备成纳米混悬剂。
仪器和原料
细匀浆器F6/10-8G(上海弗鲁克流体机械制造有限公司);高压均质机NanoDeBEE(苏州微流纳米生物技术有限公司);激光粒度分析仪Zerasizer Nano ZS90(英国Malvern Instruments公司);紫外分光光度计TU-1810S(北京普析通用仪器有限公司);透射电子显微镜H-600(日本日立公司);透析袋(MW3500,美国Sigma公司);Agilent1260[安捷伦科技 (中国)有限公司]。
PDC由重庆莱美药业股份有限公司四川大学莱美联合实验室研制,其DOX购自浙江海正药业股份有限公司; 精制蛋黄卵磷脂(E80,德国Lipoid GmbH公司);泊洛沙姆188(F68,德国BASF公司);聚乙烯吡咯烷酮-K30(PVPK30,杭州恒泉开发有限公司);羧甲基纤维素钠(CMC-Na,成都科龙化工试剂);聚乙二醇400(PEG400),十二烷基硫酸钠(SDS)(天津致远化学试剂有限公司);2-羟丙基-β-环糊精(2-HP-β-CD,Aladdin industrial corporation);氯仿,二甲基亚砜(DMSO)(重庆化学试剂有限公司);异丙醇(天津市富宇精细化工有限公司);色谱甲醇和色谱乙腈(上海科丰化学试剂有限公司)。
试验方法
PDC纳米混悬液的制备取10mgPDC固体粉末,加入纯水10mL, 用速匀浆器以25000r·min−1匀浆5min进行初分散。所得初分散液置于高压均质机中,在110MPa压力下均质25min,制得纳米混悬液。稳定剂的筛选与制备条件优化分别向PDC中加入质量分数为0.05%、0.1%、0.5%、1%和2%的E80、PEG400、F68、PVPK30、CMC-Na 和2-HP-β-CD,按上述方法制备,分别测定混悬液的粒径和电位。选取加入上述稳定剂后粒径和多分散指数(polydispersity index, PI)较优组,于室温放置,分别在第5、10、15天取样测定粒径, 选取粒径较优组对应的稳定剂作为该处方的稳定剂。重新称取10份PDC,均加入选定稳定剂, 按如上方法初分散后,分别在80、110、40、180 MPa 压力下均质初分散液,在均质次数分别为5、10、15、20、25、30和35时取样, 测定粒径和PI。
纳米粒粒径及zeta电位的测定取纳米混悬液, 用纯水稀释1倍,于Zerasizer Nano ZS90测定粒径、PI和电位,每个样品测定3次,取平均值。重复性与稳定性按较优处方制备3批PDC纳米混悬液,于室温放置,分别测定各批次样品第 5、10、15、30天的粒径、PI和zeta电位。PDC纳米混悬液形态观察取适量较优处方制备的PDC纳米混悬液,滴加于覆盖碳膜的铜网上,用磷钨酸负染, 待混悬液中载液挥发后, 用透射电子显微镜(TEM)观察。放大倍数为6.0×104倍。加速电压为75kV。载药量测定 色谱条件色谱柱:ZORBAX SB-Aq C18柱,规格:250mm×4.6mm,填料粒径5μm。流动相: SDS缓冲液(SDS1.44g、磷酸0.68mL和水500mL)∶乙腈∶甲醇为47.2∶47.2∶5.6(v/v)。流速:1.0m L·min−1,柱温: 25℃,检测器:DAD,检测波长:254nm,进样量:20µL。标准曲线的制备,以纯水为溶剂, 配制系列浓度的DOX标准液, HPLC检测, 将标准溶液浓度(Y1)对峰面积(X1) 进行线性回归,得回归方程。以水和DMSO混合物(1∶49,v/v)作为溶剂,配制系列浓度的DOX标准液,于紫外(520nm)测定吸光度值,将标准溶液浓度(Y2)对吸光度(X2)进行线性回归,得回归方程。
载药量测定取适量上述较优处方制备的3个批次PDC纳米混悬液,分别于20000r·min−1离心10min,取上清液,HPLC检测,计算出游离DOX的质量浓度(B),由于DOX出峰时间为10.0556min,而PDC是大分子药物,在该色谱条件下20min内不出峰,所以该方法能够准确测定游离DOX的量。另量取PDC纳米混悬液1mL,加入DMSO溶解并定容至50mL,以相同比例水与DMSO 混合物为对照,用紫外分光光度计于520nm处测定吸光度值,计算出混悬液中DOX的总质量浓度(D)。PDC载药量(%)=(D−B)/E×100(其E为PDC质量浓度)。
实验结果
稳定剂种类及用量对PDC纳米混悬剂的粒径和表面电荷影响很大。应用PEG400和CMC-Na制备的纳米混悬液粒径和PI均较大;卵磷脂制备的纳米混悬液粒径降低,但PI均大于0.4,说明纳米粒的分散区间比较广,均不符合纳米混悬剂的要求;F68、PVPK30和2-HP-β-CD制得的纳米粒粒径均能达到300nm以下,较为理想,结果见图1。在室温放置15天,应用PVPK30制备的纳米粒粒径增至589.9±13.3nm,且纳米混悬液中出现明显絮状物;2-HP-β-CD制备的纳米粒粒径增至711.3±35.3nm,且纳米混悬液分层,上层澄清,下层鲜红;F68制备的纳米粒粒径为285.4±8.7nm,室温放置15天粒径为281.4±9.2nm,几乎没有变化,观察外观,颜色鲜红,分布均一,说明应用F68制备的混悬液能保持体系稳定。
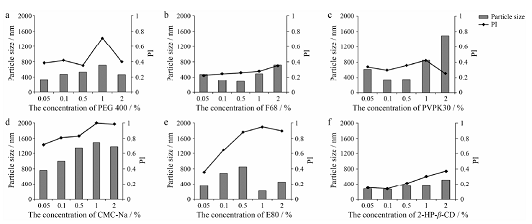
图1不同稳定剂PDC纳米混悬液的平均粒径和PI值比较
随着均质压力的增加,粒径快速减小,当压力达到110MPa,均质次数为25次时,粒径为117.0±13.2nm,PI为0.113 ±0.054;压力继续增加,粒径变化不明显。随着均质次数的增加, 粒径减小,PI明显降低, 当均质次数达到25次时,PI均小于0.2,体系分散性良好;当均质次数大于25次时,PI变化不大,结果见图2。实验发现,均质压力越高,体系产热越严重。采用先低压后高压的方法进行均质,能有效减少仪器产热。根据均质次数筛选结果,采用在80MPa条件下先均质10次,再在110MPa条件下均质25次的方法制备纳米混悬液。
3批PDC纳米混悬剂粒径均小于150nm,平均粒径为118.8±6.93nm,PI值为0.14±0.03,平均zeta电位为−27.2±0.36mV,说明优化处方制备的PDC纳米混悬剂具有很好的重复性。样品于常温下放置5、10和15天,平均粒径小于130nm,电位为−27.2±0.36mV,与0天相比变化不大,外观颜色鲜红, 体系分散均一, 无沉降和絮凝;第30天平均粒径增至178.1±14.65nm,溶液出现轻度分层,轻轻振摇后呈现良好的可重悬浮性,说明体系在30天内可以保持良好的稳定性。
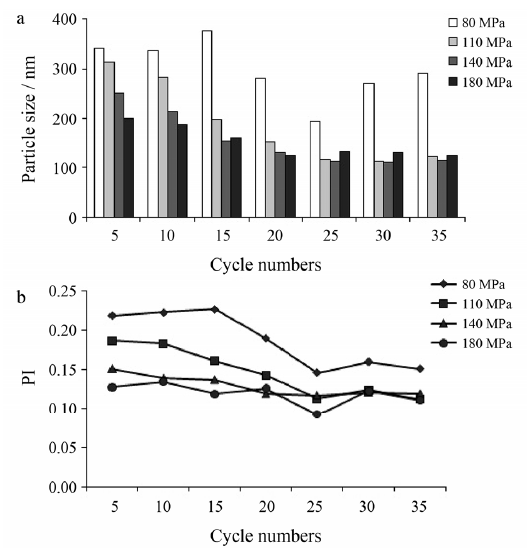
图2不同均质压力和循环次数下的平均粒径和PI值比较
 |
高压均质法制备果胶多柔比星纳米混悬剂.pdf |
下一页:静脉用纳米脂肪乳剂简介

















